清华大学罗三中课题组:电化学产生的手性α-亚胺碳正离子中间体的不对称SN1类型反应
碳正离子是有机合成中多用途中间体,可用于官能团化和构建分子骨架。碳正离子具有很高的反应活性,且具有平面结构,导致其与亲核试剂反应的SN1过程常常得到消旋化的产物。
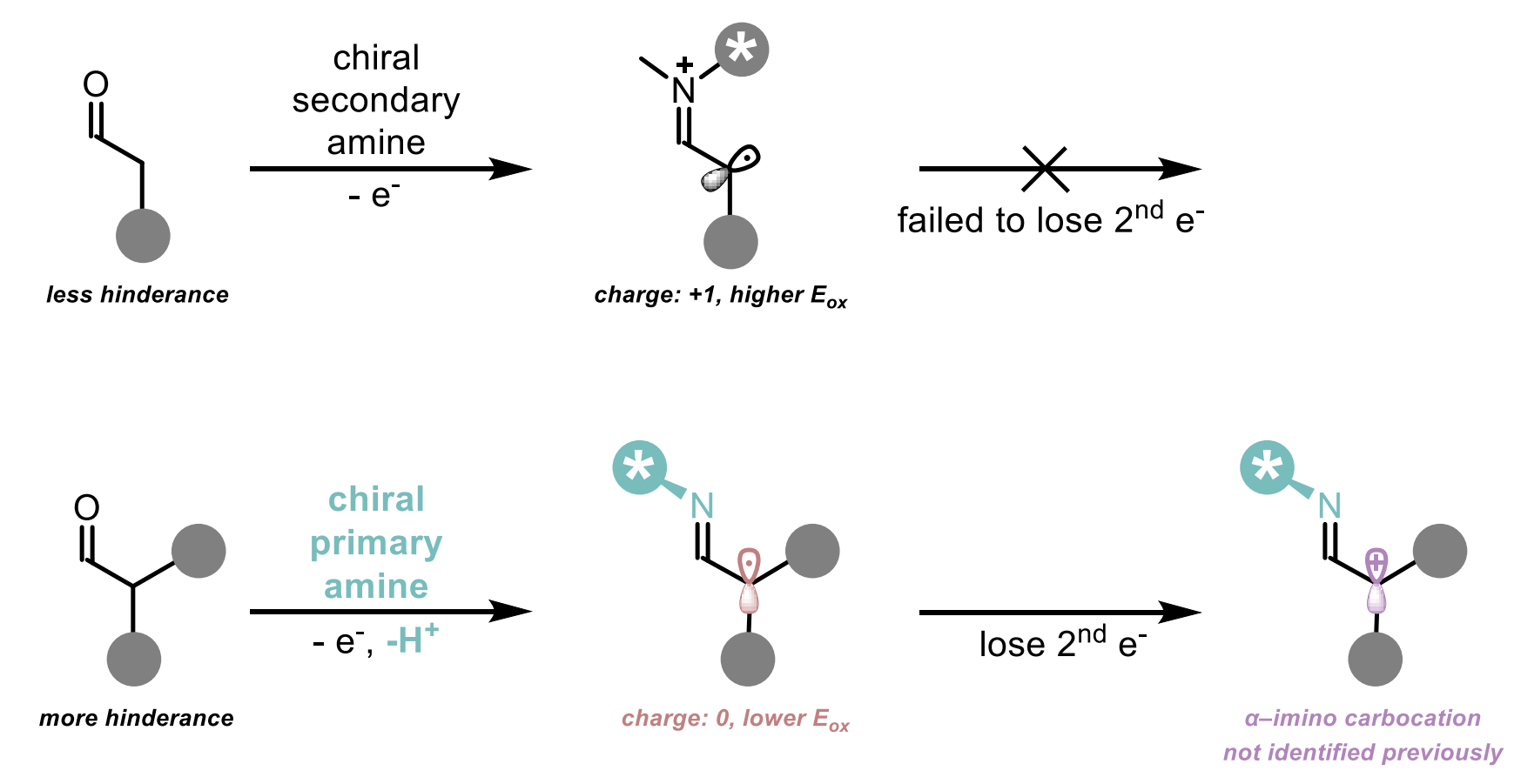
图1 伯胺催化产生 α-亚胺碳正离子
罗三中团队长期关注于研究手性氨基催化的不对称反应。团队注意到,因伯胺的氮上较之仲胺多一个质子,其形成的烯胺经历单电子氧化(SET)后,能通过失去一个质子的方式形成氧化电位更低的α-亚胺自由基中间体。团队因此设想利用手性伯胺催化与电催化结合的方式,实现羰基α-位的极性彻底反转,得到高活性的α-亚胺碳正离子中间体(图1)。
团队以α-支链醛为底物,与手性伯胺结合后,经历阳极氧化,得到α-亚胺碳正离子(图2)。得益于催化剂上的烷基结构,所得α-亚胺碳正离子外围存在局部非极性环境,即使在充满着电解质阴阳离子干扰的条件下,也能保证良好的对映选择性控制能力。团队成功实现了氧、硫、碳、氮中心亲核试剂与其的不对称SN1反应。该策略同样适用于具有复杂结构的底物醛与亲核试剂。
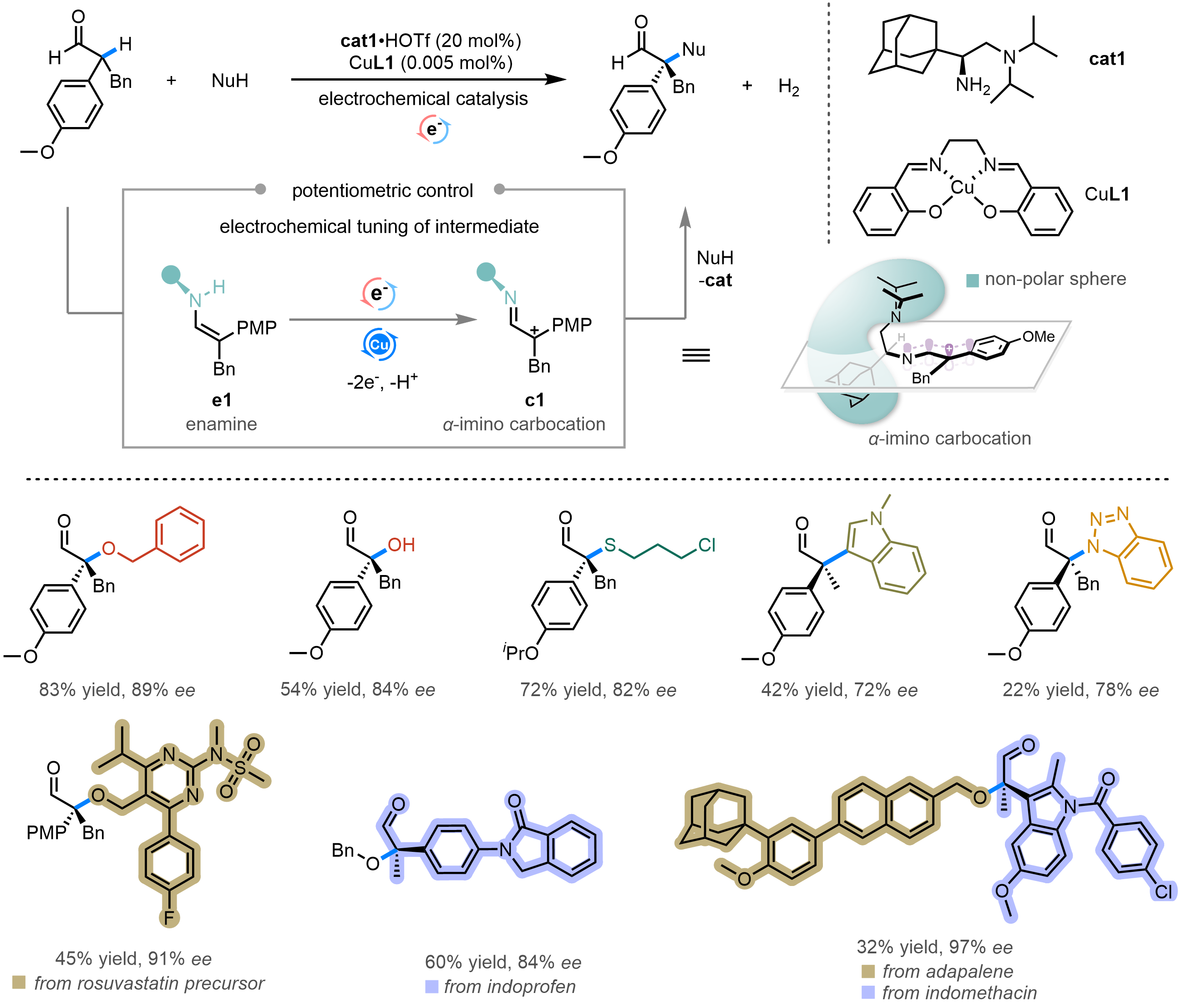
图2 电催化产生的α-亚胺碳正离子的SN1型不对称转化
团队提供了电氧化生成 α-亚胺碳正离子的实验证据。团队首先通过控制实验排除了自由基偶联路径和SN2反应路径。随后通过动力学测试发现反应初速率与苄醇浓度呈零级,符合碳正离子的动力学特征。此外还利用电喷雾质谱具备弱氧化能力的特性,实现了原位生成并表征 α-亚胺碳正离子,证明了这一中间体的存在。DFT 计算的结果说明了该反应手性控制模式为氢键诱导作用,并且E-构型的α-亚胺碳正离子较之Z-构型能量更低,并成功给出了与实验值相吻合的预测值。
近期,相关研究以“Enantioselective SN1-type reaction via electrochemically generated chiral α-Imino carbocation intermediate”为题发表在Nature Communications上。
原文链接:https://www.nature.com/articles/s41467-024-50945-2