十年磨一剑:揭秘手性富集的魔法 | 清华大学罗三中团队发展手性分子合成新途径
2022年2月25日,清华大学化学系罗三中课题组在《科学》(Science)杂志上在线发表了题为“基于烯胺光促E/Z互变的去消旋化反应”(Deracemization through photochemical E/Z isomerization of enamines)的研究文章。该工作报道了一种手性分子合成的突破性进展,通过光促中间体立体结构互变实现去消旋化,直接将手性分子一步从外消旋混合物变为光学纯。该研究为外消旋体的拆分提供了新的思路,同时也将传统氨基催化的发展应用推向新的高峰。
去消旋化反应——机遇与挑战
手性是自然界的一种基本结构属性,而生命体都是单一手性的,这就要求药物分子具有特定的手性结构。手性分子的精准构筑一直是合成化学研究前沿,也逐渐成为跨越生物、医药、材料、信息等多学科领域的关键物质构筑难题。近20年来,有三次诺贝尔化学奖授予了与手性分子合成相关的研究(2001,2018和2021)。传统上,对手性分子消旋体(含一对镜像异构体)的拆分是获得光学纯分子(单一镜像异构体)的直接方法。从1848年巴斯德分离酒石酸以来,人们发展了包括物理、化学和生物等多种消旋体拆分策略,但拆分过程目标手性分子的理论得率只有50%。最理想、最直接的合成方法,莫过于将外消旋体直接转化为该物质相应的光学纯化合物,以100%得率获得目标手性分子,这一过程被称为去消旋化反应(图1)。
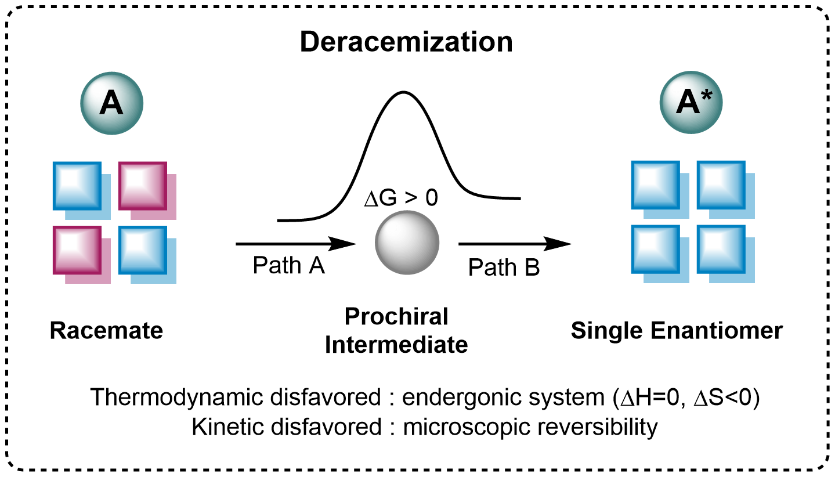
图1 去消旋化反应
然而,强大的功能也预示着研究攻关中的巨大挑战。去消旋化反应的历程大致可以分为三个阶段,即外消旋体、前手性中间体与光学纯化合物。从热力学角度来看,该反应不涉及物质结构变化,但是熵减过程,因此ΔG>0,不能自发进行。另一方面,根据微观可逆性原理,中间体的生成与转化必须是两个不同的过程,这个要求为反应路径的设计带来极大的麻烦。如何打破热力学和动力学壁垒,发展高效去消旋化策略,是手性合成一个挑战性难题。
尽管困难重重,化学家们还是发现了解决办法。既然能量不利,那就串联能量有利的反应,如氧化还原过程,以此带动去消旋化反应的进行,这也成为早期实现去消旋化反应的通用策略(图2上)。然而这个“折衷”的方法,同时向体系中加入氧化剂与还原剂,有着潜在的淬灭风险,并且当量的氧化还原副产物作为“反应能源”被“牺牲”,原子经济性不足。近期,Bach (2018)与Knowles、Miller (2019)等人先后利用光催化的能量转移与电子转移机制,实现了连烯与环脲类底物的去消旋化反应(图2下)。这些研究用光能代替化学能,为去消旋化反应提供了一个新的视角,真正意义上实现了去消旋化反应中“高原子经济性”的特点。美中不足的是,已有反应体系所使用的底物骨架较为特殊,催化体系也较为复杂。
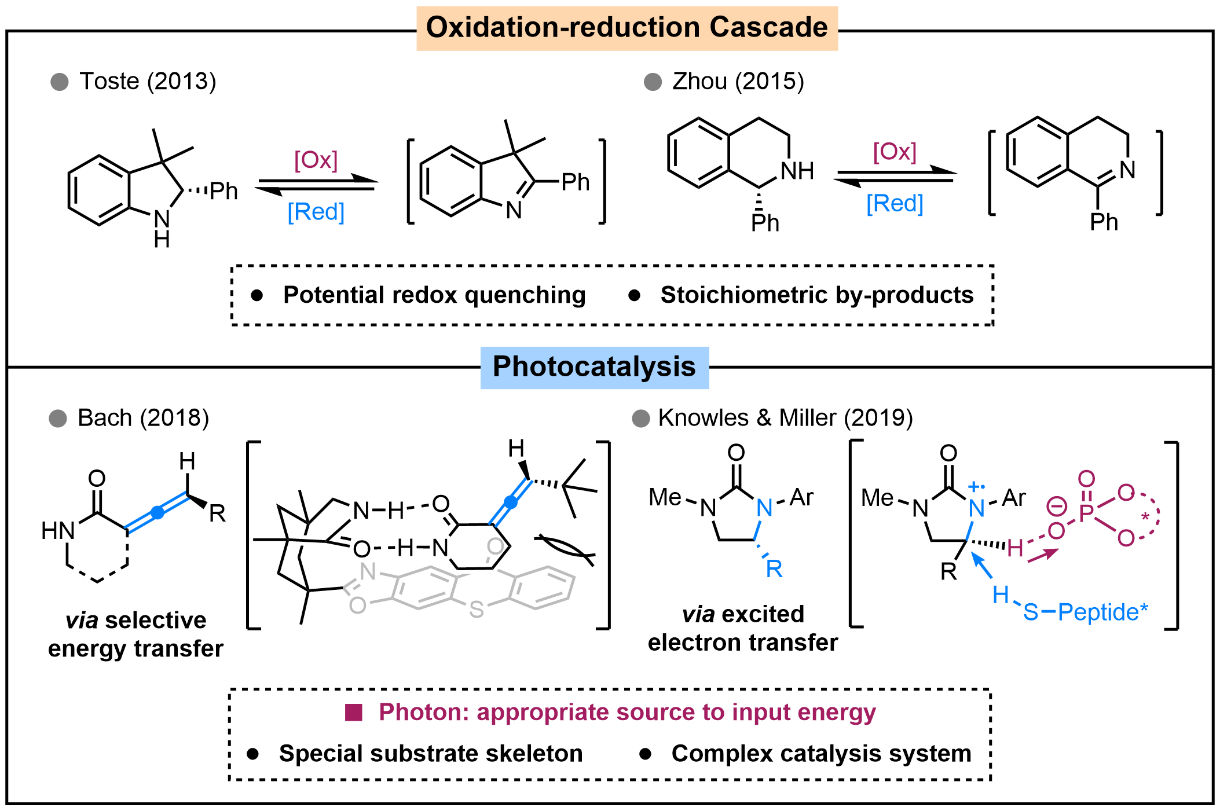
图2 去消旋化反应策略
十年磨一剑——氨基催化策略性突破
在有机催化的发展历程中,不对称氨基催化可以说是独领风骚,该领域的先驱研究者List与MacMillan也因此获得了2021年诺贝尔化学奖。清华大学罗三中课题组长期致力于仿生催化研究,开发了一类功能强大、应用广泛的仿生手性伯胺催化剂。早在2011年,该团队就发现,手性伯胺催化剂与醛类底物形成的烯胺中间体,其质子化过程有着高度的立体专一性,也就是说,烯胺的构型(E/Z)与水解产物的构型(R/S)具有一一对应的关系,这就为实现醛类底物的去消旋化带来可能。然而,尽管光学纯的醛类底物在与氨基催化剂共存时,其手性可以保持,但其外消旋体并不能实现手性富集。此后,该团队在去消旋化反应领域持续攻关,不断寻找合适的反应路径,历经坎坷,但从未放弃最初的梦想。
受到光催化去消旋化的启发,该团队设计光与烯胺催化结合的反应路线。既然烯胺的质子化过程具有高度立体专一性,那么只要能够调节烯胺的构型(E/Z),就能调控底物的手性(R/S)。尽管催化烯胺中间体的光异构化过程从未被实现,但光促烯烃的E/Z互变反应已有多例报道,这正是一个千载难逢的好机会!
光与烯胺——推开手性富集的大门
基于前期工作基础,该团队将仿生伯胺催化体系,与可见光促进能量转移联动,成功实现了α-芳基醛的高选择性去消旋化反应(图3)。该反应体系简单,条件温和,能够在1小时内达到光平衡,实现高效去消旋化。在底物骨架上修饰吸电子基、给电子基、烷基、官能团、天然产物片段、杂环等均可以获得优秀的反应效果,展现出良好的底物适用性;反应能够被放大到克量级,应用于合成一系列非甾体抗炎药物分子。
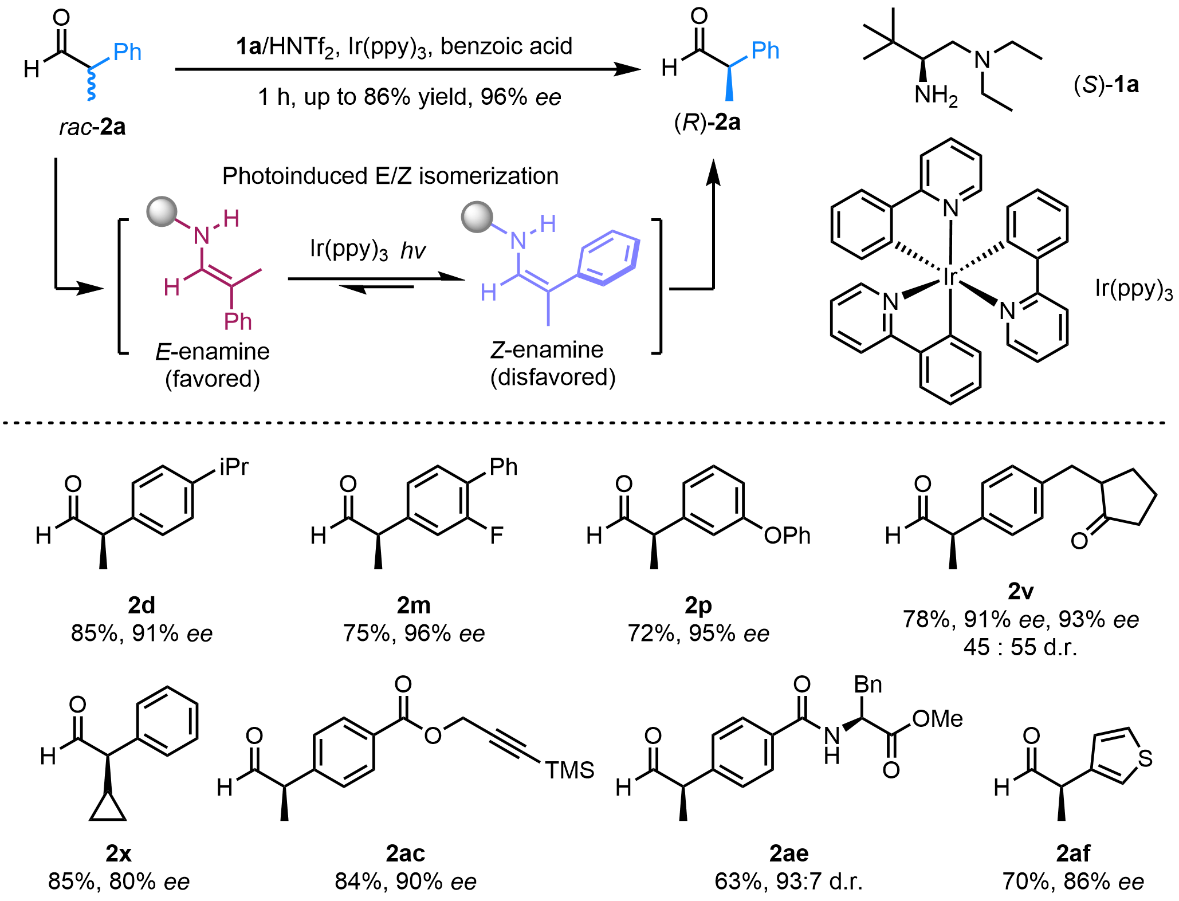
图3 基于烯胺光促E/Z互变的去消旋化反应
随后,研究团队对反应机理进行了细致的探讨。通过对比不同光敏剂能量参数与反应效果,验证了光催化能量转移的过程;通过核磁监测的烯胺生成实验,说明S构型醛与伯胺催化剂更加匹配,且适量的酸能加速醛-烯胺的平衡;通过原位光照核磁实验,该团队直接观察到了烯胺的快速E/Z互变过程,进一步支持了能量转移的机制;此外,详细的DFT计算也验证了烯胺质子化过程的立体专一性与光异构化过程的选择性。
通过总结机理证据,该团队提出了一个去消旋化手性合成的全新路径(图4):在S-构型手性伯胺催化下,S-醛优先与催化剂形成E-烯胺,随后被光异构化生成Z-烯胺,后者快速水解质子化生成R-醛。高活性S-醛不断被消耗,低活性R-醛不断富集,从而实现了去消旋化。在此过程中,光异构化提供了去消旋化反应的驱动力,适当的苯甲酸添加剂调节了达到平衡的速率,伯胺催化剂的立体专一性保证了产物的高对映选择性。
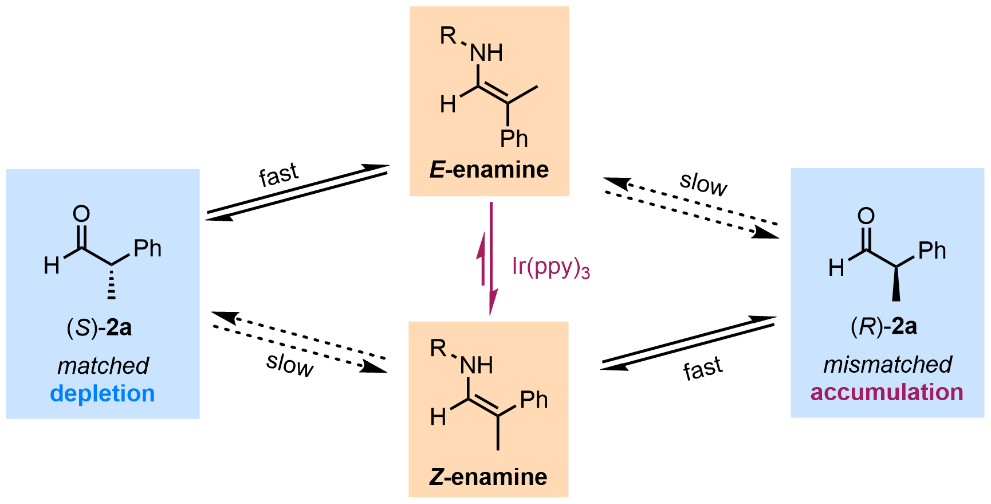
图4 去消旋化反应机理
总结与展望
把手性分子直接一步从外消旋转变为光学纯,看上去像是奇妙的魔法,实际却蕴含着精巧的设计与缜密的逻辑。去消旋化反应的热力学壁垒并不高,ΔG仅为+0.43 kcal/mol,然而,选择合适的反应路径却是难上加难,称得上是合成的艺术。罗三中团队将传统烯胺催化与光促能量转移催化巧妙结合,以十年磨一剑的坚韧,揭密了手性富集的魔法。
参考文献:
1. M. Huang, L. Zhang, T. Pan, S. Luo. Deracemization through photochemical E/Z isomerization of enamines. Science 2022,https://doi.org/10.1126/science.abl4922
2. N. Fu, L. Zhang, J. Li, S. Luo, J. P. Cheng, Chiral primary amine catalyzed enantioselective protonation via an enamine intermediate. Angew. Chem. Int. Ed. 50, 11451-11455 (2011).
3. N. Y. Shin, J. M. Ryss, X. Zhang, S. J. Miller, R. R. Knowles, Light-driven deracemization enabled by excited-state electron transfer. Science 366, 364-369 (2019).
4. A. Holzl-Hobmeier, A. Bauer, A. V. Silva, S. M. Huber, C. Bannwarth, T. Bach, Catalytic deracemization of chiral allenes by sensitized excitation with visible light. Nature 564, 240-243 (2018).